DD01은 디앤디파마텍의 지속형 기술이 접목된 주 1회 피하주사다. GLP-1 및 글루카곤 수용체에 작용한다. 1상은 107명의 환자를 대상으로 미국에서 진행됐다.
단회투여군은 제2형 당뇨를 동반한 과체중·비만 환자를 대상으로, 반복투여군은 당뇨와 비알코올성 지방간질환(NAFLD)을 동반한 비만 환자를 대상으로 진행됐다. 부작용은 기존 GLP-1 수용체 작용제에서 일반적으로 보이는 수준의 구역질과 구토 등이 일부 투여군에서 관찰됐다고 했다. 이를 통해 DD01의 안전성과 내약성을 확인했다고 설명했다.
NASH는 간에서 장기간 축적된 지방이 염증으로 발전해 간 섬유증을 유발하는 질환이다. 약물의 효율적인 간지방 제거 능력이 NASH 치료제 개발의 중요한 척도라고 했다.
약 효능에 해당하는 지방간 제거율은 위약과 DD01을 각각 주 1회씩 4주 간 반복투여해 측정했다. 투여 전후의 간내 지방량을 자기공명영상-양자밀도 지방비율(MRI-PDFF) 검사로 봤다. 그 결과 위약군은 지방량이 2.8% 감소했고 DD01 20mg 투여군에서는 19%, 40mg 투여군에서는 49.9%, 80mg 투여군에서는 52.2% 줄었다. 용량 의존적으로 단기간에 간지방을 제거할 수 있음을 확인(40mg p<0.001, 80mg p<0.0001)했다는 것이다. <br />
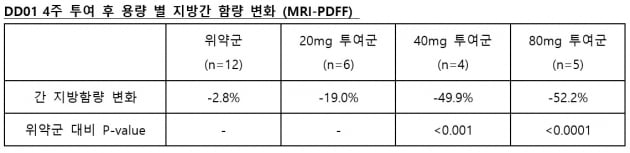
MRI-PDFF는 비침습적으로 간 내 지방량을 측정할 수 있는 검사법이다. 생검 위치에 따라 편차가 발생하는 조직생검법에 비해 높은 정확도의 정량적 측정이 가능하다고 했다. MRI-PDFF상 30%의 지방량 감소는 임상적으로 유의미한 비알코올성 지방간질환 활성 점수(NAS) 개선 및 간섬유화 지표 개선과 관련이 있다고 회사 측은 전했다.
미국 식품의약국(FDA)은 NAS 점수의 악화 없이 간섬유화를 개선하거나, 간섬유화 악화 없이 NAS 점수가 개선되는 품목을 NASH 치료제로 승인하겠다는 지침(가이드라인)을 제시하고 있다.
투여군별로 지방간 함량이 30% 이상 낮아진 환자들의 비율은 20mg에서 50%, 40mg에서 75%, 80mg에서 100%였다고 했다.
이슬기 디앤디파마텍 대표는 "4주 투약만으로 지방간질환 환자에서 50% 이상의 간지방을 제거한 임상 결과는, 현재까지 보고된 모든 NASH 치료제 후보물질들 중 가장 우수한 효능"이라며 "자세한 결과는 내달 미국 샌디에고에서 열리는 미국당뇨병학회(ADA)에서 발표할 예정"이라고 말했다.
한민수 기자 hms@hankyung.com

