9월 19~23일 주간 제약·바이오 업종 가운데 가장 많은 주목을 받은 종목은 한미약품입니다.
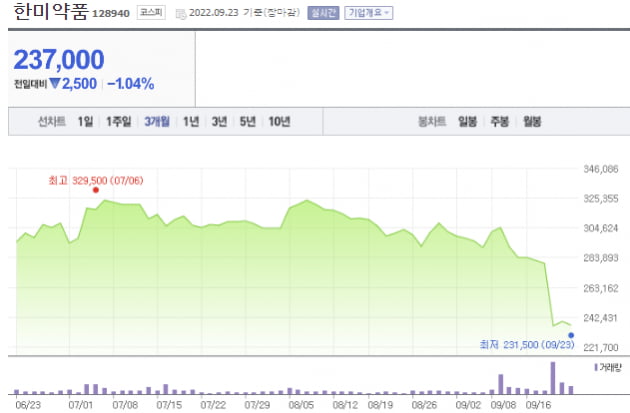
한미약품은 주당 28만4000원에 이번주 거래를 시작해 23일 23만7000원으로 한 주 거래를 마쳤습니다. 16.5% 큰 폭으로 하락했습니다. 23일에만 15.4% 급락했습니다.
한미약품 주가는 지난 13일엔 반짝 상승을 했습니다. 전 거래일 30만2000원에 거래를 마친 한미약품 주가는 장중 8% 넘게 올라 32만6500원을 찍기로 했습니다.
다만 이날 주가는 상승폭을 대부분 반납해 0.99% 상승에 그쳤습니다.
한미약품은 최근 1~2주 가장 '핫'했던 종목 가운데 하나입니다. 이 회사가 미국 파트너사인 스펙트럼에 기술이전한 신약 후보물질 2개의 희비가 엇갈렸기 때문입니다.
먼저 '희(喜)'입니다. 한미약품이 개발한 호중구 감소증 치료제 롤론티스(미국 제품명 롤베돈)가 추석 연휴였던 지난 10일 미국 식품의약국(FDA) 허가 문턱을 넘었습니다.
롤론티스는 한미약품이 지난 2012년 스펙트럼에 기술수출 후 공동개발 해온 신약입니다. 항암 치료를 받은 환자의 백혈구에서 호중구가 감소하는 질환을 치료하는 목적의 신약입니다.
서울아산병원에 따르면 호중구는 우리 몸에 침입한 혈액 내 세균이나 박테리아를 파괴하는 최전선 '방패' 역할을 합니다. 호중구가 줄어들면 감염이 쉽게 되고, 생명에 위협이 됩니다.
보통 백혈구 내 호중구 비율이 50~70%가 정상인데, 호중구의 수가 1500 이하로 떨어진 경우 호중구 감소증이라고 합니다.
롤론티스는 과립구를 자극하는 방식으로 호중구를 증가시키는 원리의 약물입니다. 이를 과립구집락자극인자(G-CSF) 계열의 약물이라고 합니다.
롤론티스는 한미약품의 자체 플랫폼 기술인 '랩스커버리'가 적용된 첫 신약이라는 점에서도 의미가 있습니다. 랩스커버리는 약효를 오랜 기간 지속시켜주는 장기지속형 플랫폼입니다.
호재에도 불구하고 주가가 소폭 반짝 상승에 그친 채 거래를 마친 건 호재가 현실화하면서 차익 실현이 일부 이뤄졌기 때문으로 풀이됩니다.
투자업계 관계자는 "롤론티스 FDA 허가 뉴스를 기다리던 투자자들이 실제 뉴스가 나오자 매도에 나섰다"고 했습니다.
실제 이날(13일) 개인이 161억원어치를 순매수했을 뿐 외국인(133억원), 기관(27억원), 심지어 투신(7억원)과 사모펀드(5억원), 기타법인(2억원)에서도 순매도를 보였습니다.
FDA 허가가 단기 호재로 기다려왔던 뉴스라면, 실제 허가가 난 이후에 대한 우려도 주가를 끝까지 밀어올리지 못한 이유로 꼽힙니다.
미국 호중구 감소증 치료제 시장은 연 3조원 규모라고 합니다. 이 시장은 미국 암젠의 신약 '뉴라티스'가 상당한 영향력을 행사하고 있는 시장입니다. 한미약품의 롤론티스는 후발주자라는 얘깁니다.
삼성증권에 따르면 8월 기준으로 뉴라티스 점유율은 13.3%이고, 뉴라티스 패치가 45.9% 점유율을 확보하고 있습니다. 암젠이 점유율 59% 이상을 확보하고 있는 것이죠. 뉴라티스 바이오시밀러(바이오의약품 복제약)도 40.8%의 점유율을 보이고 있습니다.
서근희 삼성증권 연구위원은 "후발주자인 롤론티스 판매를 맡은 스펙트럼의 영업력에 대해 우려가 크다"며 "매출 성장에는 다소 시간이 걸릴 것"이라고 코멘트했습니다.
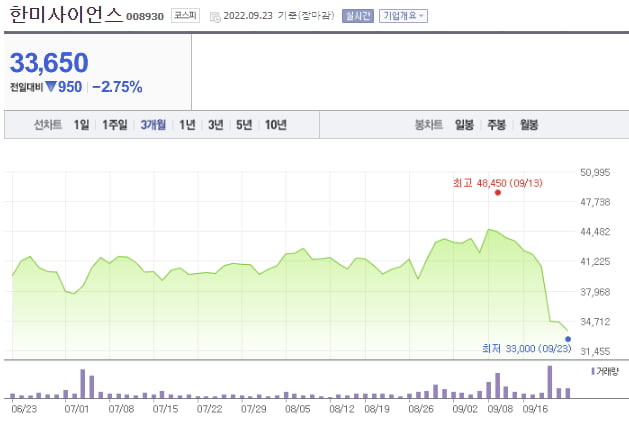
'비(悲)'는 롤론티스와 함께 또 다른 FDA 허가 기대주였던 먹는 비소세포폐암 치료제 포지오티닙의 허가 좌절 소식입니다.
FDA 항암제자문위원회(ODAC)가 23일 포지오티닙을 신속 승인해줄지 여부에 대해 표결을 한 결과 9대4의 비율로 부정적 의견이 많았습니다.
한미약품은 이런 권고 내용을 통보 받았고요. 물론 위원회의 판단은 어디까지나 권고이기 때문에 FDA의 최종 결론이 나온 건 아닙니다.
그럼에도 자문위원회의 공식적인 발표가 있기 전인 20일(현지시간) 이런 내용을 담은 브리핑 문서의 내용이 외신을 통해 전해지자 한미약품 주가는 21일 15.54% 급락했습니다.
파트너사인 스펙트럼의 주가도 37.5% 급락했습니다.
위원회가 포지오티닙에 대해 부정적 의견을 낸 건 이 약을 투약했을 때 환자가 얻을 혜택이 위험보다 크지 않다고 봤기 때문입니다.
높은 수준의 독성과 최적화되지 못한 용량 등이 원인으로 지목됐습니다.
로이터통신이 보도한 FDA 자료에 따르면 "만약 포지오티닙이 신속승인을 권고 받는다면 지금까지 승인 받은 폐암 치료제 가운데 가장 덜 효과적일 것"이라는 내용이 담겼습니다.
톰 리가 스펙트럼 최고경영자(CEO)는 위원회 회의 결과에 큰 실망감을 나타냈습니다. FDA는 오는 11월 24일까지 최종 결정을 내릴 예정입니다.
허혜민 키움증권 연구원은 "포지오티닙에 대한 기대감이 높지 않았던 상황에서 주가 하락은 향후 허가 불발 예상, 재료 소멸 인식 등 투자심리 이슈가 더 크게 반영된 것”이라고 평가했습니다.
한재영 기자 jyhan@hankyung.com



