백신 접종 개시 후 임상 대상 모집 어려워져…해외 임상 추진도
(서울=연합뉴스) 김잔디 기자 = 신종 코로나바이러스 감염증(코로나19) 치료제를 개발하는 국내 제약사들이 임상 절차와 대상 환자 모집의 어려움 등으로 인해 속도를 내지 못하고 있다. 일부는 임상 시험 환자 모집을 위해 해외로 눈을 돌리고 있다.
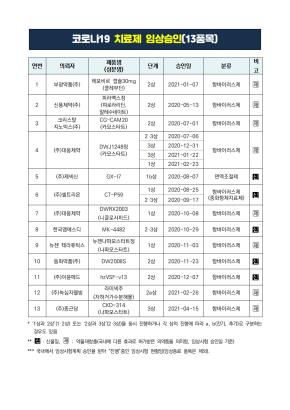
18일 식품의약품안전처에 따르면 국내에서 코로나19 치료제로 임상시험을 승인받아 진행 중인 품목은 총 13개다.
이 중 크리스탈지노믹스[083790], 동화약품[000020], 이뮨메드, 녹십자웰빙 등은 코로나19 치료제 임상시험 승인을 받았으나 실제 환자에 대한 약물 투여가 이뤄지진 않았다.
크리스탈지노믹스는 지난해 7월 식약처로부터 카모스타트의 코로나19 치료 효과를 확인하는 임상 2상 시험을 승인받았다. 애초 100명 규모로 진행할 예정이었으나 국내 유행 상황의 변화 등으로 인해 환자를 모집하지 못했다.
동화약품은 지난해 11월 'DW2008S'를 코로나19 치료제로 개발하는 임상 2상 시험을 승인받은 후 임상시험수탁기관(CRO) 선정 등 후속 절차에 적잖은 시간이 소요됐다.
동화약품 관계자는 "CRO 선정을 올해 1월에 완료했고 이후 임상을 진행할 의료기관을 확보해왔다"며 "아직 환자 모집은 시작하지 못했다"고 말했다.
지난해 12월 임상시험 승인을 받은 이뮨메드 역시 국내에서는 환자를 모집하거나 투약을 시작한 단계는 아니라고 밝혔다. 대신 러시아와 인도네시아, 이탈리아에서는 순조롭게 진행되고 있다고 덧붙였다.
안병옥 이뮨메드 대표는 "약물은 준비돼 있으나 아직 국내에서 환자에 투약하지는 않았다"며 "병원 3곳을 확보했고 임상시험 실시기관을 추가하는 등 준비 작업을 하고 있다"고 말했다.
녹십자웰빙은 올해 2월 태반주사제 '라이넥'의 코로나19 치료 효과를 확인하는 임상 2상 계획을 승인받았지만 환자 모집을 시작하지 않았다.
업계에서는 국내 코로나19 환자가 다른 나라에 비해 상대적으로 적은 데다 백신 접종이 시작돼 임상 환자 모집이 쉽지 않으리라고 전망한다.
한 제약업계 관계자는 "환자 수도 많지 않은데 머지않아 백신 접종도 본격화되면 임상 환자 모집이 더 어려워질 것 같다"고 말했다.
이 때문에 일부 제약사들은 해외로 눈을 돌려 임상시험 대상자를 모집할 전망이다. 실제 종근당[185750]은 식약처로부터 '나파벨탄'을 코로나19 치료제로 개발하는 임상 3상 시험을 승인받은 뒤 신속한 환자 모집을 위해 유럽, 브라질, 러시아, 인도 등에서 글로벌 임상을 추진하겠다고 밝혔다.
jandi@yna.co.kr
(끝)
<저작권자(c) 연합뉴스, 무단 전재-재배포 금지>


