기억과 인지 기능에 관여하는 유전자 손상을 복구하는데 핵심 역할을 하는 `노화 억제` 효소를 미국 MIT(매사추세츠 공대) 과학자들이 발견했다.
알츠하이머병 환자뿐 아니라 일반적인 고령자도, 이 효소가 감소하는 사례가 자주 관찰된다.
HDAC1으로 불리는 이 효소가 결핍된 생쥐는 나이가 들었을 때 특정한 유형의 DNA 손상이 축적됐다.
MIT 과학자들은 이 효소를 활성화하는 약물을 생쥐에 투여해 손상된 DNA의 복구와 인지 기능 개선 효과도 일부 확인했다.
이 효소의 복원이 알츠하이머병 환자는 물론이고 인지 기능이 떨어진 고령자에게도 도움을 줄 수 있다는 걸 시사한다.
연구를 수행한 차이 리-후에이(Li-Huei Tsai) 신경과학 교수팀은 관련 논문을 저널 `네이처 커뮤니케이션스(Nature Communications)`에 20일 발표했다.
논문의 수석저자이자 MIT 피카우어 학습 기억 연구소의 소장인 차이 교수는 "HDAC1이야 말로 진정한 노화 억제 분자인 것 같다"라면서 "인간의 모든 신경 퇴행 질환이 노화 과정에서 생기기 때문에 앞으로 적용 범위가 매우 넓을 것"이라고 말했다.
차이 교수팀은 2013년 HDAC1 효소와 뇌 신경세포(뉴런) DNA 복구의 연관성을 주제로 하는 두 편의 논문을 발표했다.
이번 연구에선 HDAC1을 매개로 하는 뉴런의 DNA 복구가 실패했을 때 어떤 일이 벌어지는지 알아봤다.
뇌의 뉴런과 성상교세포(astrocyte)에서 HDAC1을 제거한 생쥐는 태어나서 처음 몇개월 동안 DNA 손상 수위와 일상 행동에서 별다른 변화를 보이지 않았다.
그러나 나이가 많이 들면 차이가 확연해졌다.
HDAC1이 없는 생쥐는 DNA 손상이 쌓이기 시작했고, 시냅스 가소성(synaptic plasticity)을 조절하는 능력도 일부 상실했다. 시냅스 가소성은 뉴런과 뉴런 사이의 연결 강도 변화를 말한다.
HDAC1가 없는 늙은 생쥐는 또한 기억과 길 찾기 테스트에서도 기능 장애를 드러냈다.
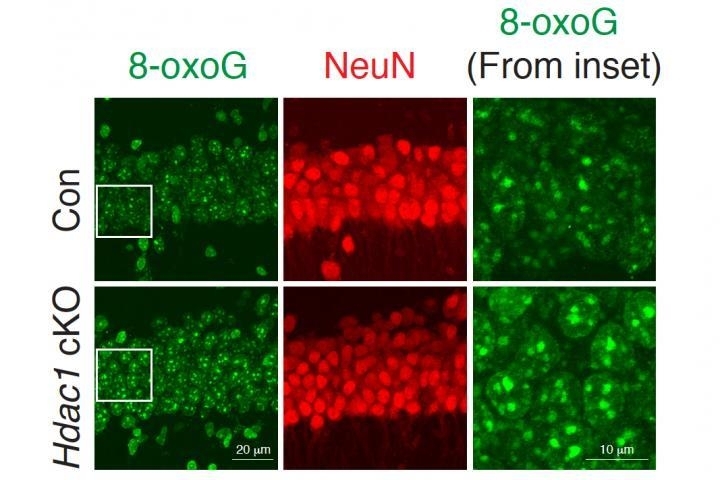
HDAC1의 결핍은 특징적으로 DNA 산화 손상을 많이 유발했다. 이런 유형의 DNA 손상은 특히 알츠하이머병 환자에서 자주 발생한다.
실제로 DNA 산화 손상을 복구하는 건 OGG1이라는 효소였다. 하지만 OGG1을 활성화하려면 HDAC1이 필요하다는 게 이번 연구에서 밝혀졌다.
시냅스(신경연접부)의 기능에 중요하게 작용하는 이온 채널의 생성 코드를 가진 유전자는 대부분 이런 유형의 손상에 취약했다.
연구팀은 HDAC1 효소와 DNA 손상이 타우 단백질의 형성에도 관여하는지를 밝히는 데 주력하고 있다.
뒤엉킨 타우 단백질은 알츠하이머병과 다른 신경 퇴행 질환의 원인 물질로 추정된다.
(사진=연합뉴스)

