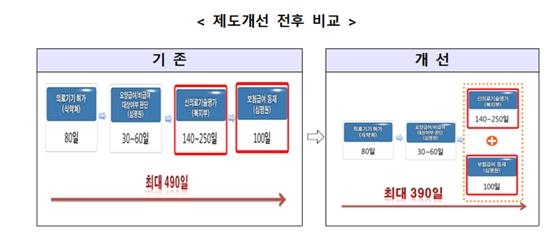
길게는 490일 걸리던 신개발 의료기기 시장 진입 기간이 최대 390일로 100일 가량 단축됩니다.
보건복지부는 신의료기술평가와 보험등재심사를 동시에 진행하도록 돕는 `신의료기술평가에 관한 규칙` 개정안을 이달 9일부터 다음달 16일까지 40일 동안 입법예고 한다고 7일 밝혔습니다.
현재 기존의 새로운 의료기술이 포함된 신개발 의료기기가 보험 적용을 받으려면 식품의약품안전처 허가 이후에도 요양급여·비급여 대상확인과 신의료기술평가 등을 거쳐야 합니다.
이 기간은 최대 490일로 이 때문에 신기술의 시장 진입이 늦어진다는 지적이 있었습니다.
그러나 개정안이 시행되면 신의료기술평가 시 한국보건의료연구원에 보험급여 등재를 위한 자료를 제출하면 건강보험심사평가원의 보험등재심사도 자동으로 진행됩니다.
신의료기술평가가 완료될 때 보험급여 등재심사도 종료돼 전체 기간이 최대 390일로 100일가량 단축되는 것입니다.
한편, 이번 개정안에 대해 의견이 있는 단체 또는 개인은 다음달 16일까지 복지부 의료자원정책과로 의견을 제출하면 됩니다.

