현대차증권은 26일 에이비엘바이오의 협력사인 컴패스테라퓨틱스가 담도암 임상 2상에서 '게임체인저'급 중간결과를 발표했다고 분석했다.
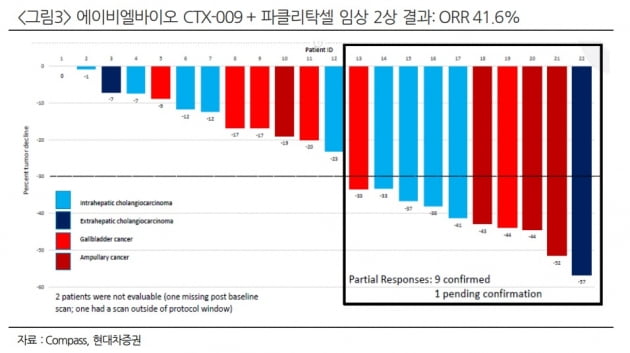
에이비엘바이오가 컴패스에 기술이전한 진행성 담도암 이중항체 'CTX-009(ABL001)'는 2상 중간결과에서 24명의 환자에 대해 객관적반응율(ORR) 41.6%를 기록했다. 2상은 표준치료에 내성이 생긴 진행성 담도암 환자를 대상으로 한다. 유효성에 있어 경쟁사 대비 우위에 있는 결과란 설명이다.
마땅한 치료제가 없는 담도암에서 최근 아스트라제네카가 발표한 'PD-L1' 항암제 임핀지와 젬시타빈 및 시스플라틴 삼중병용 3상 결과는 ORR은 26.7%였다. 'DLL4·VEGF' 이중항체 경쟁사인 온세르나는 나비시시주맙·파클리탁셀 임상 1b상에서 난소암 환자를 대상으로 43%의 부분 관해를 보여 ABL001과 유사한 유효성을 나타냈다.
엄민용 연구원은 "애브비의 'ABT-165'는 파클리탁셀·PD-1항체 병용 임상 1·1b상과 'FOLFIRI' 또는 아바스틴 병용 대장암 2상은 조기 종료돼 연구 현황이 파악되지 않고 있는 상황"이라며 "DLL4·VEGF 담도암 치료제로는 에이비엘바이오가 독보적인 효력과 임상 속도 내고 있는 상태"라고 말했다.
담도암의 1차 차료제는 젬시타빈과 시스플라틴 병용요법이 현재 표준치료제다. 표준치료의 ORR은 26.1%다. 2차 치료제는 여러 방법이 사용되며 대표적으로 폴폭스가 쓰인다. 그러나 폴폭스는 2차 치료 3상에서 ORR 5%, 무진행생존기간 중앙값(mPFS) 0.9개월 연장 등의 미미한 효과로 미충족 의료 수요가 높다고 했다.
컴패스는 임상 2상 1단계에서 파클리탁셀 병용을 진행하고 있다. 이번 결과 발표로 컴패스의 시가총액은 1개월 간 90.3% 급증했다.
엄 연구원은 "ABL001은 기술이전 후 임상개발이 순항 중"이라며 "올 3분기 글로벌 임상 2·3상, 4분기에 난소암 2상이 개시될 예정이며 난소암도 긍정적 결과 보일 것"이라고 기대했다.
사노피에 1조3000억원 규모로 기술이전한 파킨슨병 치료제 외에도, 에이비엘바이오의 이중항체 기술력을 검증할 주요 임상들이 지속될 예정이라 주목할 필요가 있다는 판단이다.
한민수 기자 hms@hankyung.com

